무세포 시스템에서 유전자로부터 단백질 합성하는 것은 살아있는 세포를 사용하는 것에 비해 독특한 접근 방식을 제공합니다. 과정은 다음과 같습니다.
- 1. 무세포 추출물(Lysate)의 제조
- 첫 번째 단계에서는 세포 추출물을 생성합니다. 이것은 본질적으로 세포 용해물, 즉 열린 세포를 부수고 막과 세포 잔해를 제거하여 만들어진 현탁액입니다.
- 추출물은 리보솜, 운반 RNA(tRNA), 아미노산, 번역 과정에서 필요한 시작, 연장 및 종료에 관여하는효소를 포함하여 단백질 합성에 필요한 필수 요소를 보유합니다.
- 무세포 단백질 합성은 일반적으로 대장균(E. coli), 밀 배아(Wheat germ) 및 토끼 망상적혈구(Rabbit reticulocyte)의 용해물이 사용되며, 각각의 용해물은 사용자가 원하는 단백질에 따라 장점과 한계가 있습니다.
- 2. DNA template 확보
- Plasmid : 원형의 DNA로, 무세포 시스템에서 효율적인 전사를 위한 조절 요소를 갖도록 변형할 수 있습니다. Plasmid는 대량의 단백질이 필요할 때 자주 사용됩니다.
- PCR product : 원하는 유전자 서열이 포함된 특정 DNA fragment만 PCR을 통해 증폭하여 무세포 단백질 합성에 사용할 수 있습니다. 이 접근법은 plasmid 구성보다 빠르지만 단백질 양이 더 적을 수 있습니다.
- 필요로 하는 단백질을 암호화하는 DNA template가 필요합니다. DNA template는 주로 두 가지가 사용됩니다.
- 3. In vitro transcription(IVT)
- DNA template에서 mRNA를 합성하는 과정이 포함됩니다. 여기서 정제된 RNA polymerase는 DNA template 및 rNTP(A, U, C, G)과 함께 무세포 추출물에 도입됩니다.
- RNA polymerase는 DNA의 프로모터 서열을 인식하고 이를 사용하여 유전자를 상보적인 mRNA로 전사합니다. 이 mRNA는 단백질 합성을 위한 유전 정보를 담고 있습니다.
- 4. 무세포 번역
- 합성된 mRNA는 번역에 필요한 모든 요소를 포함하는 무세포 추출물을 통해 번역됩니다.
- 추출물의 리보솜은 mRNA의 시작 codon(AUG)을 인식하고 단백질 합성을 시작합니다. 특정 아미노산을 운반하는 tRNA는 mRNA codon과 상호 작용하고 리보솜은 mRNA 서열에 따라 아미노산을 함께 연결합니다.
- 이 과정은 mRNA의 정지 codon에 도달하면 종료되고 번역 종결인자(release factor)가 결합하여 리보솜에서 완성된 단백질을 방출합니다.
무세포 단백질 합성의 장점
- 속도 및 편이성: 무세포 시스템은 세포 배양을 활용한 기존 방법에 비해 더 빠르고 효율적인 접근 방식을 제공합니다.
- 확장성: 반응량과 성분을 조정하여 단백질 생산량을 쉽게 조정할 수 있습니다.
- 순도: 무세포 시스템에서 합성된 단백질은 일반적으로 세포 배양 과정에서 생성되는 오염 물질이 없습니다.
무세포 단백질 합성의 응용
- 신속한 단백질 생산: 이 기술은 단백질 기능 연구 또는 단백질 활성 스크리닝과 같은 연구 목적에 유용합니다.
- 막 단백질 생산: 무세포 시스템은 살아있는 세포에서 발현하기 어려운 막 단백질을 생산하는 데 합니다.
- 체외 진단: 무세포 단백질 합성은 항체 검출을 위한 특정 항원을 발현함으로써 진단 도구를 개발하는 데 사용될 수 있습니다.
- 생물제조: 다양한 응용 분야를 위한 복합 단백질의 생산 가능성을 제시합니다.
Q1: 코돈 최적화 (Codon Optimization)란 무엇이며, 왜 필요한가요?
코돈 최적화는 목표 아미노산 서열은 그대로 유지하면서, 해당 아미노산을 코딩하는 DNA 염기 서열(코돈)을 전략적으로 변경하여 유전자 발현 효율, 안정성, 합성 용이성 등을 향상시키는 과정입니다. 이는 단순한 코돈 변경을 넘어, 유전자의 전반적인 성능을 개선하는 핵심적인 합성생물학 기술입니다. Bioneer의 GeneCrafter™는 이러한 최적화를 수행하는 강력한 도구입니다.
최적화의 필요성:
- 코돈 사용 빈도 편향 (Codon Usage Bias, CUB) 극복:
- 대부분의 아미노산은 여러 개의 코돈으로 암호화될 수 있지만, 생명체마다 특정 코돈을 선호하는 경향(CUB)이 있습니다. 예를 들어, Serine 아미노산을 코딩하는 UCU, UCC, UCA, UCG 코돈 중 특정 생명체는 특정 코돈(들)만 효율적으로 사용합니다.
- 인간 유전자를 박테리아에서 발현시키는 등 이종 시스템(Heterologous System)에서 유전자를 발현시킬 때, 이러한 CUB 차이는 mRNA 번역(translation) 효율을 크게 저하시켜 목표 단백질 생산량을 감소시킬 수 있습니다. GeneCrafter™는 타겟 숙주(Target Host)의 CUB에 맞춰 코돈을 최적화하여 번역 효율을 극대화합니다.
- 문제 서열 제거 및 기능성 향상:
- 반복 서열 (Repeats): 단순 반복(Homopolymers, 예: AAAAAA)이나 복잡한 반복 서열은 유전자 합성 오류를 유발하거나 유전자의 불안정성(예: 재조합)을 증가시킬 수 있습니다.
- mRNA 2차 구조 (Secondary Structure): mRNA 분자가 스스로 접혀 헤어핀(Hairpin) 같은 복잡한 구조를 형성하면, 리보솜의 접근을 방해하여 번역 개시(translation initiation)를 저해하거나 번역 속도를 느리게 할 수 있습니다. 특히 5' UTR 영역의 구조는 매우 중요합니다.
- 제한 효소 자리 (Restriction Enzyme Sites): 특정 제한 효소 인식 서열은 유전자 클로닝, 유전자 회로(Genetic Circuit) 조립 등 후속 실험 과정에 제약을 줄 수 있습니다.
- CpG/UpA 다이뉴클레오티드: 특히 mRNA 백신 및 치료제 개발 시, 특정 다이뉴클레오티드는 면역 반응을 유발하거나 mRNA 분해를 촉진할 수 있습니다.
- 기타 조절 모티프: 전사/번역 관련 조절 서열(예: TFBS, Shine-Dalgarno 서열), 잘못된 스플라이싱 신호(Cryptic Splice Sites), Poly-A 신호 등이 코딩 서열 내에 존재하면 의도치 않은 결과를 초래할 수 있습니다.
- 유전자 서열 내에는 합성 또는 발현 과정에 문제를 일으킬 수 있는 다양한 요소들이 숨어있을 수 있습니다.
- GeneCrafter™는 이러한 문제 서열들을 식별하고 제거하여 유전자 합성 성공률을 높이고, 예측 가능한 유전자 발현 및 안정적인 기능을 보장합니다. 또한, 백신 개발 시 특정 서열을 변경하여 약독화(Attenuation)하는 데에도 활용될 수 있습니다.
GeneCrafter™ 최적화의 이점:
- 예측 가능하고 높은 수준의 유전자 발현: 타겟 숙주에 최적화된 코돈과 안정적인 mRNA 구조를 통해 단백질 또는 mRNA 생산량을 극대화합니다.
- mRNA 안정성 및 기능성 향상: mRNA 분해를 유발하는 서열을 제거하고 안정적인 구조를 형성하여 In Vitro Transcription(IVT) 효율을 높이고, 번역 효율을 개선하며, mRNA 기반 약물(백신, 치료제)의 효능을 증대시킵니다.
- 유전자 합성 성공률 향상 및 비용 효율성 증대: GC 함량 불균형, 반복 서열, 헤어핀 구조 등 합성을 어렵게 만드는 요소들을 제거하여 더 빠르고 안정적으로 유전자를 합성할 수 있게 하며, 이는 경쟁력 있는 가격으로 이어집니다.
- 이종 시스템에서의 발현 최적화: 서로 다른 종 간의 유전자 발현 장벽을 극복하고, 원하는 시스템에서 유전자가 안정적으로 기능하도록 설계하는 데 필수적입니다.
Q2: GeneCrafter™를 이용한 유전자 최적화 서비스를 받을 수 있나요?
Bioneer는 자체 개발한 GeneCrafter™ 소프트웨어를 이용하여 고객 맞춤형 코돈 최적화(Codon Optimization) 및 약독화(Attenuation) 서비스를 무료로 제공하고 있습니다.
서비스를 요청하시려면 다음 정보를 geneorder@bioneer.co.kr로 보내주십시오.
- DNA 또는 단백질(Protein) 서열: 최적화할 대상 서열 (FASTA 형식 권장)
- 타겟 숙주 (Target Host/Organism): 유전자가 발현될 생명체 (예: E. coli K12, Homo sapiens, CHO-K1, S. cerevisiae)
- 제외할 제한 효소 (Restriction Enzymes to Avoid): 후속 클로닝 또는 실험에 사용될 제한 효소 목록 (선택 사항)
- 주요 응용 분야 (Application): 최적화 목적 (예: 단백질 발현, mRNA 생산, 백신 개발)
- CAI 약독화 (CAI Attenuation): 번역 효율을 의도적으로 낮추고자 할 경우 (선택 사항, 수준 지정 가능)
Q3: GeneCrafter™란 무엇인가요?
GeneCrafter™는 Bioneer가 자체 개발한 최첨단 코돈 최적화 및 약독화 소프트웨어입니다. 단순한 코돈 치환을 넘어, 유전자 발현, 안정성, 합성 효율 등에 영향을 미치는 다양한 생물학적, 물리화학적 요인들을 종합적으로 고려하는 다목적 최적화(Multi-Objective Optimization) 알고리즘을 기반으로 합니다. 고객의 유전자 최적화 요청 시, GeneCrafter™를 사용하여 최상의 결과를 제공합니다.
Q4: 기존 코돈 최적화 방식과 GeneCrafter™의 차이점은 무엇인가요?
기존의 코돈 최적화는 주로 단일 목표(Single-Objective), 즉 타겟 숙주의 코돈 사용 빈도(CUB)를 일치시켜 번역 효율을 높이는 것에 집중하는 경우가 많았습니다.
반면, GeneCrafter™는 훨씬 더 포괄적이고 정교한 다목적 최적화(Multi-Objective Optimization) 접근 방식을 사용합니다. 이는 마치 여러 악기를 조화롭게 연주하여 최상의 하모니를 만드는 것과 같습니다. GeneCrafter™는 다음과 같은 다양한 목표들을 동시에 고려하고 균형을 맞춥니다.
- 코돈 사용 빈도 (Codon Usage Bias, CUB): (기본) 타겟 숙주가 선호하는 코돈을 사용하여 번역 효율을 높입니다. (GeneCrafter는 단순 빈도뿐 아니라 코돈 문맥 효과도 고려할 수 있습니다.)
- GC 함량 (GC Content): (안정성 & 합성) 전체 및 국소적(Local) GC 함량을 적절한 범위로 조절하여 DNA/mRNA의 과도한 안정성(높은 GC) 또는 불안정성(낮은 GC) 문제를 해결하고 합성 성공률을 높입니다.
- mRNA 2차 구조 (mRNA Secondary Structure): (효율성 & 안정성) mRNA가 스스로 접혀 번역을 방해하는 헤어핀(Hairpin) 등의 구조 형성을 최소화합니다. 특히 번역 개시 부위(Translation Initiation Site) 주변 구조를 최적화하여 리보솜 접근성을 높입니다.
- 회피 서열 모티프 (Sequence Motifs to Avoid): (기능성 & 안전성)
- 제한 효소 인식 자리: 클로닝 및 유전자 조작의 유연성을 확보합니다.
- 불안정성 유발 서열: (예: AREs) mRNA가 조기에 분해되는 것을 방지합니다.
- 비정상적 전사/번역 신호: (예: Cryptic Splice Sites, Prokaryotic RBS) 의도치 않은 유전자 발현 조절이나 처리를 막아 예측 가능성을 높입니다.
- 반복 서열 (Repeat Sequences): (안정성 & 합성) 단순 반복(Homopolymers), 직렬 반복(Tandem Repeats), 복잡한 내부 반복 등을 제거하여 유전자 합성 오류를 줄이고 유전적 불안정성(Genetic Instability)을 방지합니다.
- 코돈 쌍 빈도 (Codon Pair Bias, CPB): (번역 속도 & 정확성) 특정 코돈 쌍이 연속될 때 번역 속도나 정확성에 영향을 미치는 것을 고려하여, 번역 과정을 미세 조정하고 단백질 접힘(Protein Folding)에 영향을 줄 수 있습니다.
- 면역원성 감소 (Reduced Immunogenicity): (안전성 - 특히 mRNA) mRNA 백신/치료제 등 체내 전달 응용 분야에서 중요합니다. CpG, UpA 다이뉴클레오티드 빈도 조절, dsRNA(이중 가닥 RNA) 형성 가능성이 있는 역반복 서열(Inverted Repeats) 제거, 특정 면역 자극 모티프(TLR agonist sequences 등) 회피 등을 통해 원치 않는 선천성 면역 반응(Innate Immune Response)을 최소화합니다.
결론적으로, GeneCrafter™는 단순 CUB 최적화를 넘어, 유전자의 설계-구축-테스트(Design-Build-Test) 사이클 전반에 걸쳐 발생할 수 있는 문제들을 미리 예측하고 해결하는, 합성생물학 연구를 위한 강력하고 신뢰성 높은 솔루션입니다.
바이오니아의 ExiProgen™은 자동화된 단백질 합성 및 핵산 추출을 위해 특별히 설계된 시스템입니다. 이는 본질적으로 연구 환경 내에서 이러한 프로세스를 단순화하고 합리화하는 투인원(two-in-one) 도구입니다. 주요 기능은 다음과 같습니다.
- ExiProgen은 무세포 단백질 합성 방식을 활용합니다. 이는 살아있는 세포에 의존하지 않고 단백질 생산을 위한 필수 요소(리보솜, tRNA, 아미노산 등)를 포함하는 특별히 준비된 추출물에 의존한다는 것을 의미합니다.
- 시스템은 완전히 자동화되어 있습니다.
- 필요한 시약과 키트 구성품을 추가합니다.
- 관심 단백질을 인코딩하는 DNA template(plasmid 또는 PCR product)을 주입합니다.
- ExiProgen은 DNA template에서 IVT를 통해 mRNA를 생성하고 이후 mRNA를 단백질로 번역하는 전체 프로세스를 처리합니다.
무세포 시스템은 본질적으로 살아있는 세포 외부의 단백질 합성을 모방하는 생명공학 및 연구에 사용되는 강력한 도구입니다. 개념을 정리하면 다음과 같습니다.
- 전통적인 단백질 합성:
- 살아있는 세포에서 단백질 합성은 세포 내부에 있는 복잡한 기계를 사용하여 세포질 내에서 발생합니다.
- 이 프로세스에는 두 가지 주요 단계가 포함됩니다.
- 전사(DNA -> mRNA): 핵의 DNA가 청사진 역할을 합니다. RNA polymerase라고 불리는 효소는 DNA 서열을 단일 가닥 메신저 RNA(mRNA)로 복사합니다.
- 번역(mRNA -> 단백질): mRNA는 유전적 지시를 세포질의 단백질 생성 공장인 리보솜으로 전달합니다. 리보솜은 mRNA 코드를 사용하여 아미노산을 특정 단백질 서열로 조립합니다.
- 무세포 시스템:
- 무세포 시스템에서는 전체 세포가 필요하지 않습니다. 이는 시험관 내에서 단백질 합성에 필요한 필수 세포 구성 요소를 포함하는 단순화된 환경을 제공합니다.
- 이러한 구성 요소는 일반적으로 세포를 부수고 막과 기타 세포 잔해를 제거하여 만든 현탁액인 세포 용해물에서 파생됩니다.
- 나머지 추출물은 단백질 생산에 중요한 기계를 유지합니다.
- 무세포 시스템의 유형:
- 세포 추출물 기반: 이 시스템은 대장균, 밀 배아 또는 토끼 망상적혈구와 같은 다양한 소스의 용해물을 활용합니다. 각 소스는 원하는 단백질에 따라 장점과 한계가 있습니다.
- 정제된 효소 기반: 이 시스템은 리보솜, 효소 및 tRNA와 같은 정제된 구성 요소를 사용하여 반응 조건을 보다 효과적으로 제어할 수 있습니다.
- 무세포 시스템의 이점:
- 속도 및 단순성: 살아있는 세포를 배양하는 것에 비해 무세포 시스템은 단백질 합성에 더 빠르고 효율적인 접근 방식을 제공합니다.
- 확장성: 반응량과 성분을 조정하여 단백질 생산을 쉽게 확장하거나 축소할 수 있습니다.
- 순도: 무세포 시스템에서 합성된 단백질은 일반적으로 전체 세포에 존재하는 오염 물질이 없습니다.
- 직접 조작: 시스템을 통해 반응 조건을 더 쉽게 조작할 수 있습니다. 연구자들은 비표준 아미노산을 도입하거나 특정 목적을 위해 반응 매개변수를 수정할 수 있습니다.
- 무세포 시스템의 응용:
- 신속한 단백질 생산: 이 기술은 단백질 기능 연구 또는 단백질 활성 스크리닝과 같은 연구 목적에 유용합니다.
- 막 단백질 생산: 무세포 시스템은 살아있는 세포에서 발현하기 어려운 막 단백질을 생산하는 데 유리할 수 있습니다.
- 체외 진단: 무세포 단백질 합성은 항체 검출을 위한 특정 항원을 발현함으로써 진단 도구를 개발하는 데 사용될 수 있습니다.
- 생물제조: 이 접근법은 다양한 응용 분야를 위한 복합 단백질의 미래 생산 가능성을 제시합니다.
다음은 무세포 시스템에서 히스티딘 태그(His-tag)를 사용한 단백질 정제에 대한 분석입니다.
His 태그가 붙은 단백질을 이용한 무세포 단백질 합성:
- His-Tag가 있는 DNA 구조: 관심 있는 단백질을 암호화하는 DNA 구성으로 시작합니다. 이 DNA 서열은 종종 단백질의 N 말단(시작) 또는 C 말단(끝)에 히스티딘 잔기 문자열(His-tag)을 코딩하는 서열을 포함하도록 조작됩니다.
- 무세포 단백질 합성:
- 번역에 필요한 기계와 함께 세포 추출물이 포함된 무세포 시스템을 사용하여 DNA template에서 단백질을 합성합니다.
- 번역하는 동안 리보솜은 원하는 단백질 서열과 함께 His-tag를 통합하여 mRNA 서열을 번역합니다.
His-Tag를 이용한 단백질 정제:
- 고정화 금속 친화성 크로마토그래피(IMAC):
- 이는 His 태그가 붙은 단백질을 정제하는 가장 일반적인 기술입니다.
- 니켈(Ni) 이온으로 코팅된 비드가 포함된 크로마토그래피 컬럼을 사용합니다.
- 바인딩 및 세척:
- His 태그가 붙은 단백질을 함유한 무세포 반응 혼합물을 크로마토그래피 컬럼을 통과시킵니다.
- His 태그가 붙은 단백질은 비드의 니켈 이온과 특이적으로 결합하는 반면, 혼합물의 다른 단백질은 컬럼을 통해 흘러 폐기물로 수집됩니다.
- 그런 다음 비특이적으로 결합된 분자를 제거하기 위해 세척 단계를 수행합니다.
- Elution: 정제된 His 태그가 붙은 단백질을 Elution하기 위해 경쟁 분자(주로 이미다졸)가 더 높은 농도로 포함된 용액이 도입됩니다. 이미다졸은 니켈 이온과 결합하기 위해 His 태그와 경쟁하여 His 태그가 붙은 단백질이 비드에서 분리되어 정제된 단백질 분획으로 수집됩니다.
무세포 시스템에서 His-Tag 정제의 장점:
- 특이성: His-tag는 복잡한 무세포 추출물에서 관심 단백질을 분리하는 구체적이고 효율적인 방법을 제공합니다.
- 단일 단계 정제: IMAC는 상대적으로 간단하고 빠른 기술로 무세포 반응 혼합물에서 단일 단계 정제를 제공합니다.
- 호환성: 무세포 시스템은 일반적으로 His-tag 정제 방법과 호환됩니다.
- His-Tag 절단(선택 사항): 어떤 경우에는 정제 후 His-Tag를 제거해야 할 수도 있습니다. 이는 His-tag와 단백질 사이의 링커 서열을 절단하는 특정 효소를 사용하여 달성할 수 있습니다.
- 최적화: 사용된 특정 단백질 및 무세포 시스템에 따라 IMAC 조건(예: 용리를 위한 이미다졸 농도)의 일부 최적화가 필요할 수 있습니다.
발현하고자 하는 단백질의 gene을 합성한 후에 ExiProgen™으로 단백질을 발현시킨 후 정제하여 보내 드리는 서비스입니다.
발현하고자 하는 단백질을 coding하는 gene을 단백질 합성용 키트에 첨가하여 ExiProgen™ 장비에 장착하고 매뉴얼대로 가동하면, 손쉽게 정제된 단백질을 얻을 수 있습니다.
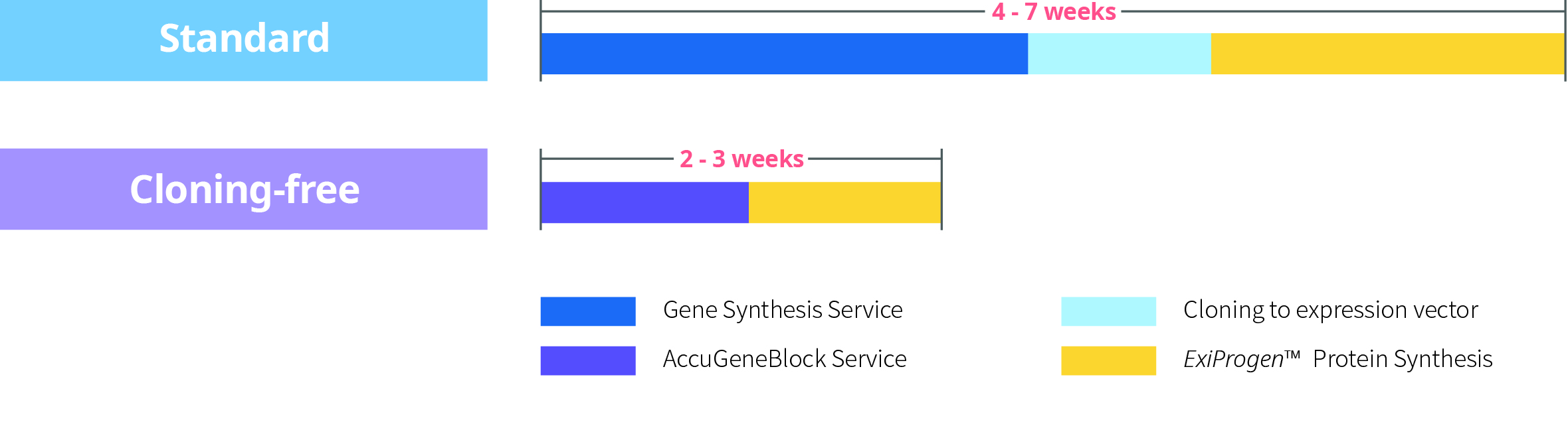
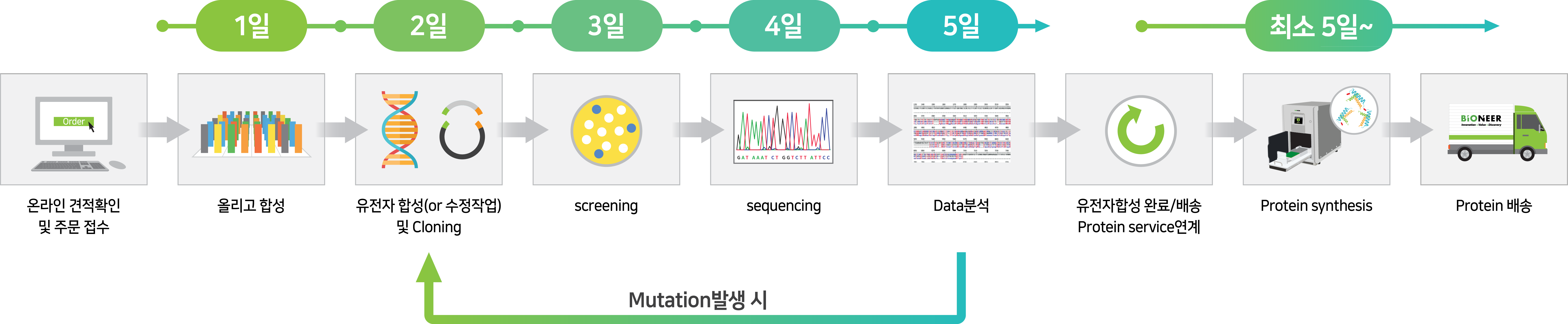
Standard Gene to Protein Service는 gene 합성 (300 bp~3000 bp) 후에 gene이 expression vector (pBT7-N-His or pBT7-C-His)에 cloning된 plasmid 형태로 단백질 합성용 키트에 첨가하여 protein 합성을 진행하는 서비스입니다.
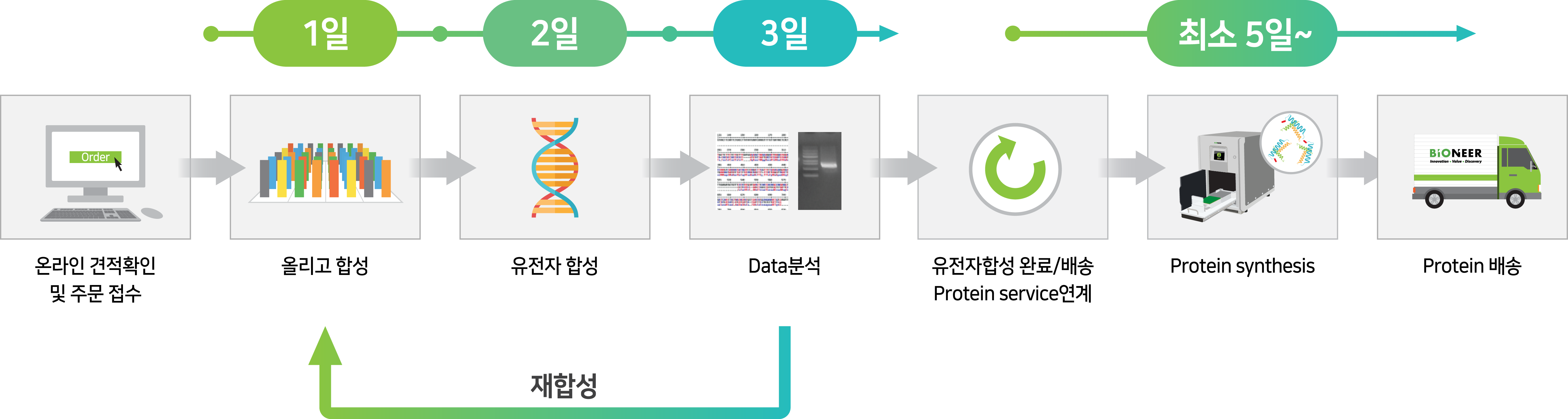
Cloning-free Gene to Protein Service는 AccuGeneBlock 서비스 (300 bp~1000 bp) 후에 gene을 PCR product형태로 단백질 합성용 키트에 첨가하여 Protein 합성을 진행하는 서비스입니다.