Oligonucleotide 합성기에서 가장 보편적으로 사용되는 합성방법은 Koster에 의해 개발된 cyanoethyl phosphoramidite를 이용하여 DNA 구조의 골격을 이루는 phosphodiester 결합을 연결해가는 ‘phosphite triester’ 방법이다(Nucl. Acids Res. 1984, 12, 4539; Tetrahedron Lett. 1983, 24,5843). 이를 통해 짧은 시간에 Oligonucleotide를 높은 효율로 합성할 수 있으며 (합성효율: >98%) 합성 시 사용되는 phosphoramidite monomer는 coupling을 위해 활성화되기 전에는 상당히 안정되어 있어 장기 보관도 가능합니다.
합성 과정은 nucleoside가 부착된 고형지지체로부터 시작하여 deblocking, coupling, oxidation, capping 과정으로 이루어지는 cycle 을 반복함으로써 원하는 염기서열의 Oligonucleotide를 얻게 된다. <그림 1 참조>
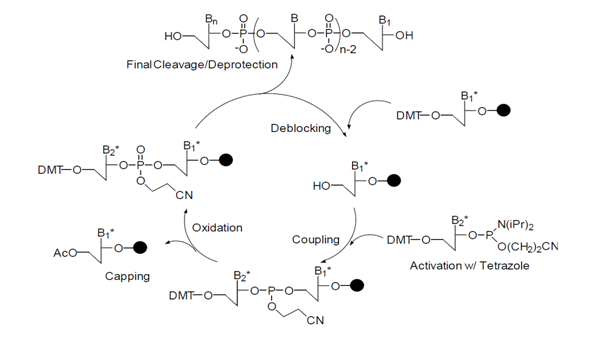
(1) Deblocking
합성 cycle의 첫 단계인 deblocking 과정은 고형지지체에 붙어 있는 염기의 5’OH의 보호기인 DMT기를 떼어내는 반응으로, 산성 조건이 요구되어 보통 3% trichloroacetic acid 를 사용한다. 한편 산성 조건 하에서는 purine계열 염기와 sugar ring 사이의 결합이 끊어지는 depurination 반응이 일어날 수 있으며 특히 염기가 adenosine 인 경우에는 그 경향이 더 심할 수 있다고 보고되었다. Trichloroacetic acid 는 매우 강한 산으로 (pKa : ~1.5) deblocking 에 사용할 때 depurination 시킬 가능성이 있어 너무 오랫동안 deblocking 반응을 하지않도록 주의가 요구된다. 상기의 문제점을 최소화하기 위해 trichloroacetic acid 대신 약한 산인 dichloroacetic acid 가 쓰여지기도 한다. Deblocking 시 고형지지체로부터 떨어져 나가는 DMT 양이온은 진한 주황색을 띄는데 이의 흡광도를 통해 올리고 합성 시의 결합효율을 측정하는 데에 이용할 수 있다.
(2) Coupling
Deblocking 과정을 통해 생성된 고형지지체내의 5'-hydroxyl 기는 가해주는 nucleoside phosphoramidite monomer 와 coupling 반응을 통해 원하는 염기서열의 Oligonucleotide 를 합성하게 된다. 이때 사용되는 nucleoside phosphoramidite monomer는 그림2에서 보듯이 염기부분의 amine 기는 보통 benzoyl 기(adenosine, cytidine 경우) 또는 isobutyryl 기로(guanosine 경우) 보호되어 있으며 모든 monomer 는 5’-hydroxyl 기가 DMT로 보호되어 있어 계속되는 결합반응의 연결부분 역할을 하게 된다. <그림 2 참조>
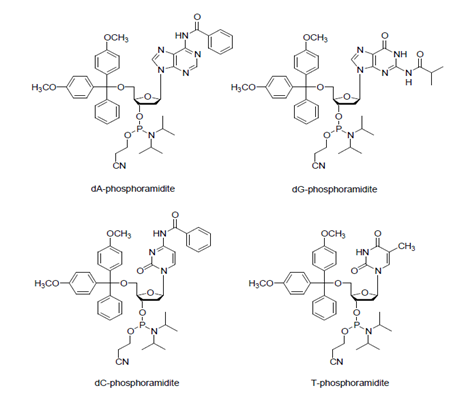
사용되는 phosphoramidite 구조 그 자체로는 상당히 안정되어 있으므로 고형지지체의 5’-hydroxyl 기와 결합하기 위해서는 활성화 과정이 필요하다. 보편적으로 사용되는 activator 로는 tetrazole 로서 phosphoramidite 와 반응하여 nitrogen 부분을 protonation 시킨 뒤 diisopropyl amino 기를 치환시켜 매우 반응성이 강한 tetrazolide구조로 변환시킨다.
결과적으로, 반응성이 강한 tetrazolide와 고형지지체의 5’-hydroxyl기 간의 결합반응을 통해 Oligonucleotide의 phosphite triester 결합이 되는데 이때 약간의 수분이라도 존재하면 반응성이 강한 tetrazolide와 반응하여 원하지 않는 부산물을 생성하여 합성수율을 저하시키기 때문에 coupling과정에서는 무수 조건이 필수적이다..
(3) Oxidation
Phosphoramidite 와 5’-hydroxyl 기의 coupling 과정을 거쳐 생성된 phosphite triester 구조는 더 안정된 phosphate triester로 변환시키는 과정이 필요하게 된다. 이를 위해서는 iodine을 사용한 oxidation 반응이 사용되며 결과적으로 phosphite는 phosphate로 바뀌게 된다.
(4) Capping
Coupling 반응은 정량적으로는 일어나지는 않기 때문에 (보통 >98%) coupling 후 고형지지체에는 반응하지 않은 5'-hydroxyl기가 남아있게 되는데 이런 올리고가 다음 cycle의 coupling 과정에 반응하게 되면, 한 개의 염기가 deletion 된 배열을 갖는 (N-1)mer 를 생성하는 원인이 된다.
이렇게 deletion된 올리고들은 합성완료 후 원하는 Oligonucleotide의 정제를 어렵게 만들기 때문에 이를 제거하는 것이 중요하다. 그래서 coupling 과정 후 반응하지 않은 올리고의 5’-hydroxyl기를 더 이상 반응하지 않게 ‘capping’ 할 필요가 있다. 이를 위해 acetic anhydride와 N-methylimidazole을 사용하여 acetylation시킴으로써 반응하지 않고 남아있는 고형지지체내의 5'-hydroxyl기를 capping시키게 된다.
원하는 길이의 Oligonucleotide의 합성은 상기의 과정들을 반복하여 실시함으로써 이루어지며 합성이 완료되면 최종적으로 ammonia 처리를 하여 합성된 Oligonucleotide를 고형지지체로부터 떼어낸 뒤 정제과정을 거쳐 순수한 Oligonucleotide로 얻게 된다.